لماذا تضعف المناعة عند مرضى السكري؟ دراسة حديثة تكشف الآلية الجزيئية
لطالما عرفنا أن السكري يضعف الجسم، لكن العلم اليوم يغوص إلى أعماق الخلية ليكشف لنا أن جزيئات الطاقة التي نعتمد عليها قد تكون هي الخنجر الذي يطعن جهازنا المناعي من الخلف. تبدأ القصة من عملية التحلل السكري التي درسناها في المدرسة، لتنتهي باكتشاف طبي مذهل يفسر لنا لماذا يسقط مرضى السكري ضحية للمضاعفات الفيروسية الشديدة مثل كوفيد-19.
كشفت دراسة منشورة في Cell Press أن ارتفاع سكر الدم يزيد إنتاج البيروفات داخل الخلايا، ما يؤدي إلى تعديل بروتين «STAT1» وإضعاف مسار الإنترفيرون المناعي المسؤول عن مقاومة الفيروسات.
التحلل السكري: من الجلوكوز إلى البيروفات
إذا عدت بذاكرتك إلى أيام الأحياء في المدرسة الثانوية، فغالبًا ستتذكر مسارًا مهمًا يُسمى التحلل السكري «Glycolysis». وهو إحدى العمليات الأساسية التي تشرح كيف تُنتج الخلايا الطاقة من الجلوكوز. يوجد هذا المسار في معظم الكائنات الحية، ويمثل الخطوة الأولى لاستخدام الكربون مصدرًا للطاقة.
باختصار: يتم تكسير جزيء جلوكوز واحد عبر عدة خطوات حتى يتحول في النهاية إلى جزيئين من البيروفات «Pyruvate». بعد ذلك، يعتمد مصير البيروفات على توفر الأكسجين: إذا كان الأكسجين متوفرًا، يدخل البيروفات إلى الميتوكوندريا ويكمل عبر مسار آخر يسمى دورة حمض الستريك «TCA cycle»، ليتحول إلى «Acetyl-CoA» لإنتاج كميات أكبر بكثير من الطاقة. أما إذا لم يتوفر الأكسجين، فإن الخلية تحول البيروفات إلى لاكتات كحل بديل للحفاظ على إنتاج الطاقة.
كل هذه الخطوات تتحكم بها إنزيمات مهمة مثل: «Hexokinase» و«Phosphofructokinase» و«Enolase» و«Pyruvate kinase».
أحد أهم الإنزيمات في هذا المسار هو إنزيم «Pyruvate kinase M2» «PKM2»، الموجود في معظم أنسجة الجسم، ويؤدي دورًا كبيرًا في تنظيم سرعة التحلل السكري. ووظيفته هي تحويل «phosphoenolpyruvate» إلى «pyruvate»، مع إنتاج «ATP» في الوقت نفسه.
لكن أهمية البيروفات لا تقتصر فقط على كونه ناتجًا نهائيًا لإنتاج الطاقة، بل له أيضًا دور في الحفاظ على توازن الخلية. وأي خلل في مستواه أو وظيفته يرتبط بأمراض مثل السكري من النوع الثاني والسرطان.
لاحظ الباحثون، من خلال متابعتهم أحدث الدراسات العلمية، وجود مجال متزايد يشير إلى أن نواتج الأيض لا تقتصر فقط على إنتاج الطاقة، بل يمكنها التأثير مباشرة في البروتينات وتغيير وظائفها. فعلى سبيل المثال، يمكن للاكتات «المشتق من البيروفات» أن يرتبط بالبروتينات ويُحدث تعديلًا يسمى «Protein lactylation»، وهو يؤثر في عمليات مثل: إصلاح الحمض النووي «DNA repair»، والمناعة الفطرية، ونمو الأورام.
وكان العلماء يعرفون مسبقًا أن البيروفات يمكنه الارتباط بالسكريات في كائنات مثل البكتيريا والخمائر عبر عملية تسمى «Saccharide pyruvylation»، لكن لم يكن واضحًا ما إذا كان هذا النوع من التعديل يمكن أن يحدث في بروتينات الإنسان أيضًا.
اكتشاف Pyruvylation: النوع الجديد من التعديلات البروتينية
أدى ذلك إلى دراسة نُشرت في مجلة «Cell Press» بعنوان: «Pyruvate is a natural suppressor of interferon signaling by inducing STAT1 protein pyruvylation».
وكان هدف الدراسة الإجابة عن سؤال مهم: هل يستطيع البيروفات الارتباط مباشرة بالبروتينات وتغيير وظائفها من خلال نوع جديد من التعديلات بعد الترجمة «PTM»؟
وبالفعل، أكدت الدراسة وجود تعديل بروتيني جديد يسمى «Protein pyruvylation». كما ربطت الدراسة هذا الاكتشاف بمرض السكري، خصوصًا حالات ارتفاع سكر الدم «Hyperglycemia».
لاحظ الباحثون أن مرضى السكري أكثر عرضة للمضاعفات الشديدة عند الإصابة بفيروس «COVID-19» الناتج عن فيروس «SARS-CoV-2»، لكن التفسير الجزيئي الدقيق لذلك لم يكن واضحًا سابقًا. وحاولت الدراسة تفسير العلاقة بين ارتفاع سكر الدم والعدوى الفيروسية على مستوى أعمق داخل الخلية.
الآلية الجزيئية: كيف يعطل السكر مسار الإنترفيرون؟
كانت الآلية المقترحة كالتالي:
عندما يرتفع مستوى الجلوكوز في الدم، تستهلك الخلايا الجلوكوز بمعدل أعلى، الأمر الذي يؤدي إلى زيادة نشاط التحلل السكري بصورة مفرطة. ونتيجة لذلك، يرتفع إنتاج البيروفات داخل الخلية بمعدل كبير. وهذه الزيادة لا تؤثر فقط في أيض الطاقة، بل تزيد أيضًا من احتمالية حدوث هذا التعديل البروتيني الجديد.
وعند هذه المرحلة، تبدأ سلسلة التأثيرات داخل جسم الإنسان:
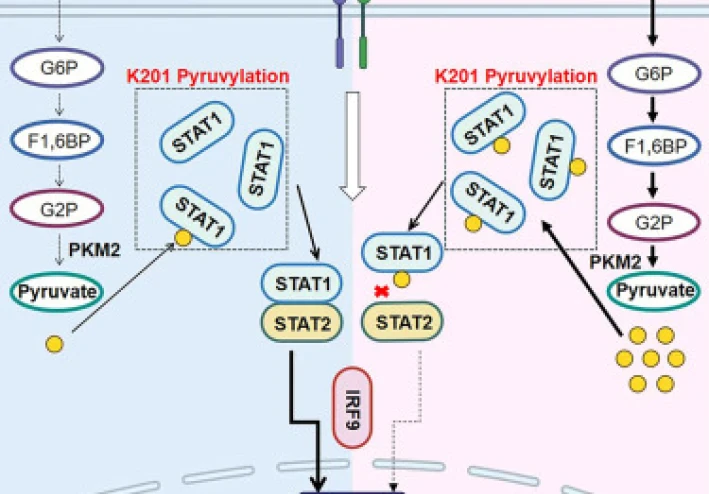
- ارتفاع الجلوكوز ← زيادة التحلل السكري ← ارتفاع مستوى البيروفات.
- ثم يبدأ البيروفات الزائد بالارتباط ببروتين مناعي مهم يسمى «STAT1»، تحديدًا عند الحمض الأميني «Lysine 201» «K201»، مكونًا تعديلًا يسمى «Pyruvylation».
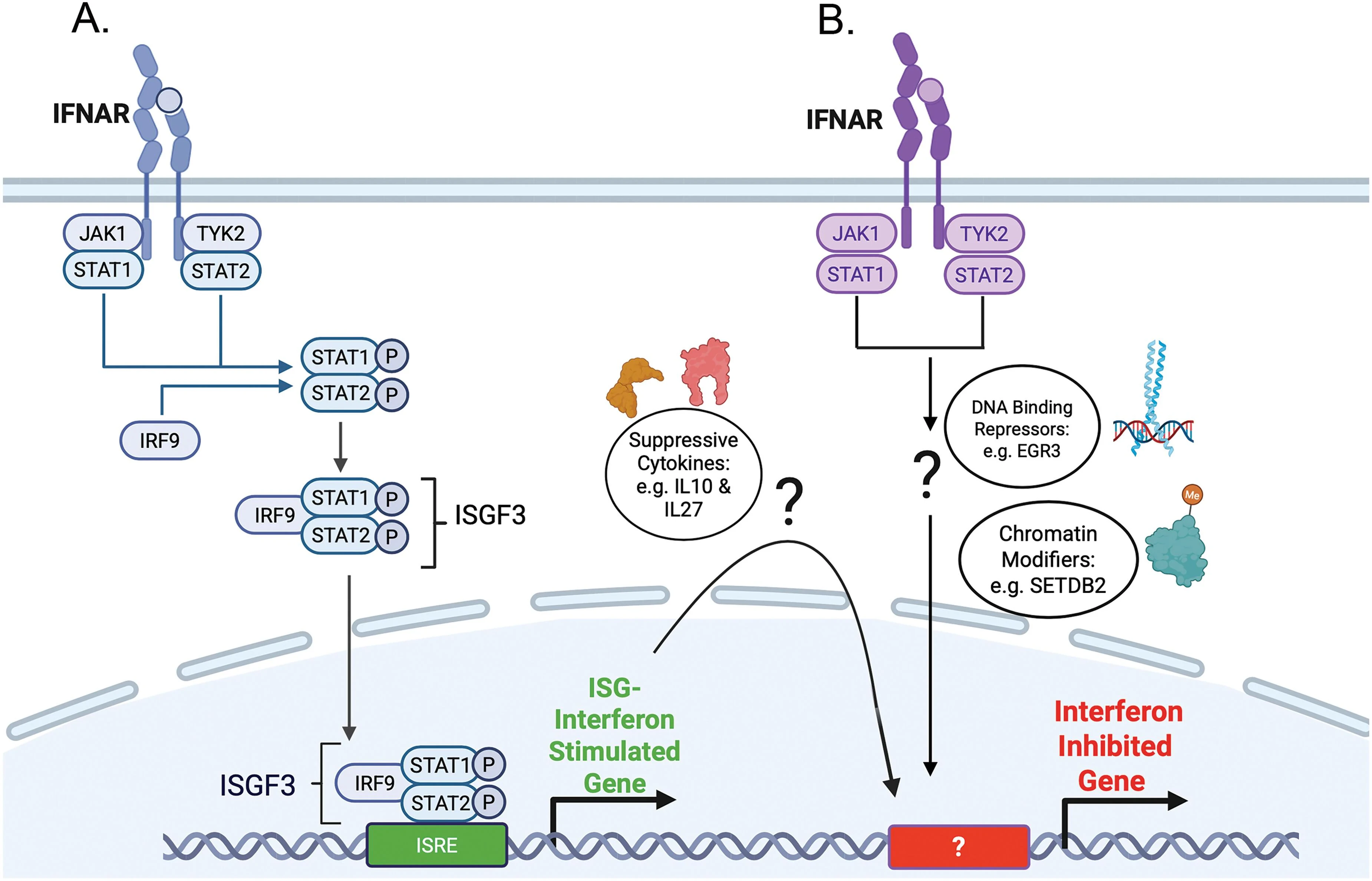
يُعد «STAT1» عنصرًا أساسيًا في مسار مناعي مهم جدًا يسمى «Type I interferon signaling» «IFN-I»، الذي يعتمد عليه الجسم لاكتشاف الفيروسات ومكافحتها. ولكي يعمل هذا المسار على النحو المطلوب، يجب أن يرتبط «STAT1» ببروتين آخر يسمى «STAT2».
لكن عندما يخضع «STAT1» لعملية «pyruvylation» عند «K201»، فإن هذا التعديل يغيِّر بنية البروتين ووظيفته، الأمر الذي يمنعه من الارتباط بـ«STAT2». ونتيجة لذلك، يتعطل مسار «IFN-I»، فتضعف الاستجابة المناعية ضد الفيروسات.
الأدلة العلمية: من الفئران إلى عينات دم البشر
وللتأكد من ذلك تجريبيًا، استخدم الباحثون فئرانًا معدلة وراثيًا تُسمى «STAT1 K201R knock-in mice»، إذ جرى تعديل موقع «K201» على نحوٍ يمنع حدوث «pyruvylation».
وأظهرت هذه الفئران مقاومة أقوى بكثير ضد الفيروسات مقارنة بالفئران الطبيعية، وهو ما أكد أن «pyruvylation» الخاص بـ«STAT1» يثبط المناعة فعلًا.
كما لوحظت الظاهرة نفسها لدى البشر. جمع الباحثون عينات دم من مجموعتين: مجموعة بمستويات جلوكوز طبيعية أقل من «6.1 mmol/L»، ومجموعة بمستويات جلوكوز مرتفعة تتجاوز «10 mmol/L» «فرط سكر الدم».
ثم حللوا الدم والخلايا المناعية المعروفة باسم «PBMCs» «Peripheral Blood Mononuclear Cells»، التي تشمل الخلايا اللمفاوية والوحيدات المهمة للدفاع المناعي.
ووجدوا أن الأشخاص ذوي السكر المرتفع لديهم مستويات أعلى من البيروفات في الدم وداخل الخلايا. وهذا منطقي؛ لأن ارتفاع الجلوكوز يزيد نشاط التحلل السكري، وبالتالي يرفع إنتاج البيروفات.
كما اكتشفوا ارتفاعًا واضحًا في مستوى «pyruvylation» لبروتين «STAT1» عند «K201»، أي إن البروتين كان أكثر تعرضًا لهذا التعديل لدى مرضى فرط السكر.
وعندما فحصوا وظيفة «STAT1»، وجدوا أنه لم يعد قادرًا على الارتباط بكفاءة مع «STAT2». وهذا الارتباط ضروري لتفعيل مسار «IFN-I» المضاد للفيروسات.
بعد ذلك، عرَّض الباحثون هذه الخلايا لـ«IFN-I» داخل المختبر لمراقبة استجابتها. في الوضع الطبيعي، تُنشِّط الخلايا مجموعة من الجينات المضادة للفيروسات تُعرف باسم:
«ISGs» «Interferon-Stimulated Genes». لكن خلايا الأشخاص ذوي السكر المرتفع أظهرت استجابة أضعف بكثير، مع انخفاض واضح في تنشيط جينات «ISGs» مقارنة بالأشخاص ذوي السكر الطبيعي.
والأهم من ذلك، وجد الباحثون علاقة عكسية واضحة بين مستوى البيروفات وتعبير «ISGs»:
كلما ارتفع البيروفات، انخفض نشاط الجينات المضادة للفيروسات. وهذا يدعم بقوة فكرة أن البيروفات ليس مجرد ناتج أيضي، بل يثبط الاستجابة المناعية مباشرةً.
والآن نعود إلى السؤال الرئيسي: لماذا يكون مرضى السكري أكثر عرضة للإصابة بالعدوى الفيروسية؟ هذا الجزء مهم جدًا طبيًا. فالمرضى الذين يعانون من ارتفاع مزمن في سكر الدم يكونون أكثر عرضة للإصابة بالفيروسات، وغالبًا ما تظهر عليهم أعراض أشد.
وتقدم هذه الدراسة تفسيرًا مقنعًا لذلك: ارتفاع الجلوكوز يزيد نشاط التحلل السكري، الأمر الذي يرفع مستوى البيروفات داخل الخلايا.
ثم يتولى البيروفات تحفيز «pyruvylation» لبروتين «STAT1» عند «K201»، فيمنع «STAT1» من الارتباط بـ«STAT2»، ويعطل مسار «IFN-I».
ونتيجة لذلك، تفقد الخلايا المناعية جزءًا كبيرًا من قدرتها الدفاعية ضد الفيروسات، وهو ما يفسر ضعف المناعة وزيادة القابلية للعدوى لدى هؤلاء المرضى.
ما علاقة ذلك بمرضى التهاب الكبد «B»؟
تناولت الدراسة أيضًا علاج فيروس التهاب الكبد «B» المزمن «Hepatitis B».
أحد العلاجات القياسية لالتهاب الكبد «B» المزمن هو استخدام:
«Type I interferon» «IFN-I»، والهدف منه تحفيز الجهاز المناعي للسيطرة على الفيروس وتحقيق شفاء وظيفي. لكن المشكلة أن معدلات الاستجابة منخفضة جدًا، نحو 10% فقط.
وهذا البحث يقدم تفسيرًا محتملًا: بعض المرضى، خصوصًا الذين يعانون من اضطرابات في أيض الجلوكوز، قد يكون لديهم ارتفاع في «STAT1 pyruvylation»، الأمر الذي يجعل إشارات «IFN-I» غير فعالة.
بمعنى آخر، حتى لو أُعطي علاج الإنترفيرون، فإن الخلية نفسها لا تستطيع الاستجابة له على النحو المطلوب؛ لأن «STAT1» قد خضع لهذا التعديل بالفعل.
وقد يفسر ذلك فشل علاج الإنترفيرون لدى كثير من المرضى.
مستقبل العلاج: نحو آفاق جديدة
تشير الدراسة إلى أنه إذا استطعنا تقليل أو منع «pyruvylation» البروتيني، فقد نتمكن من استعادة نشاط «STAT1» الطبيعي وإعادة تفعيل مسار «IFN-I».
وقد يتحقق ذلك عبر:
- تطوير جزيئات صغيرة تمنع «pyruvylation» مباشرة.
- استخدام تدخلات أيضية تقلل النشاط المفرط للتحلل السكري، خصوصًا لدى مرضى السكري، الأمر الذي يخفض مستوى البيروفات.
وفي الحالتين، سيكون الهدف هو إعادة تنشيط الاستجابة المناعية الطبيعية وتحسين فعالية العلاجات المعتمدة على الإنترفيرون.
وكأي دراسة علمية، فهذه الدراسة لها بعض القيود.
وقد أشار الباحثون أنفسهم إلى عدة أسئلة ما تزال دون إجابة:
أولًا: توجد حاجة إلى أدوات أفضل، مثل أجسام مضادة عامة لـ«pyruvylation» تستطيع اكتشاف جميع البروتينات التي تتعرض لهذا التعديل، وليس «STAT1» فقط.
ثانيًا: لا تزال الإنزيمات والعوامل التنظيمية المسؤولة عن «pyruvylation» داخل الخلايا غير معروفة، وهو أمر مهم إذا أردنا استهداف هذه العملية علاجيًا.
ثالثًا: يحتاج الباحثون إلى فهم كيف يؤثر هذا التعديل في أمراض أخرى غير العدوى الفيروسية، مثل السرطان والاضطرابات الالتهابية؛ لأن البيروفات قد يكون له دور أوسع بكثير في تنظيم وظائف الخلية.
كل هذه الأسئلة تفتح الباب أمام أبحاث مستقبلية قد تعيد تشكيل فهمنا بالكامل للعلاقة بين الأيض والمناعة.
رغم عظمة الاكتشاف، لا تزال هناك فجوات؛ فنحن بحاجة لأدوات تكتشف جميع البروتينات التي تتعرض لهذا التعديل، وفهم دور الإنزيمات المنظمة له. كما يبقى السؤال مطروحًا حول تأثير هذه العملية في أمراض أخرى كالسرطان، لذا نجد أنفسنا في النهاية بصدد إعادة تشكيل فهمنا بالكامل للعلاقة المعقدة بين ما نأكله وبين كيفية استجابة أجسادنا للأوبئة.
المصدر العلمي
https://www.sciencedirect.com/science/article/pii/S0092867426001108?utm_source